الجزيئات والذرات للسنة الثانية اعدادي 2022
مرحبا بكم أعزاءي في موقع JAMI3DOROSMAROC ، تعرفنا في الشرح الماضي : بعض خصائص الهواء ومكوناته ، على طبقات الغلاف الجوي و خصائصها ، و على الخصائص الفيزيائية للهواء و مكوناته ، أما اليوم فسنقدم لكم شرح تفصيلي لدرس الجزيئات والذرات les molécules et les atomes 2ème année collège ، سنتعرف من خلاله على التركيب الجزيئي للهواء و على الذرات و رموزها و على الصيغة الكيميائية للجزيئية و على أنواع الأجسام.

|
| الجزيئات والذرات للسنة الثانية اعدادي |
ما هو مفهوم الجزيئة؟
الجزيئة (molécule) هي أصغر جزء من المادة تتكون من عدد معين من الذرات المرتبطة فيما بينها ، و التي تكون من نفس النوع أو من أنواع مختلفة، و يمثل شكلها بالنموذج الجزيئي.
ما هو النموذج الجزيئي؟
تمثل كل جزيئة بنموذج خاص بها يسمى النموذج الجزيئي (modèle moléculaire)، حيث تمثل الذرات المكونة للجزيئة بأشكال كروية ذات أحجام و ألوان مختلفة أو متشابهة حسب نوعها.
جدول النموذج الجزيئي

|
| جدول النموذج الجزيئي |
التركيب الجزيئي للهواء
يتكون الهواء من جزيئات مختلفة و متعددة أبرزها جزيئات ثنائي الأكسجين (molécules de dioxygene) التي تشكل نسبة 20% تقريبا و جزيئات ثنائي الأزوت (molécules de diazote) التي تشكل نسبة 80% كما هو موضح بالنموذج الجزيئي التالي.

|
| التركيب الجزيئي للهواء |
يتكون الهواء بالقنينة التالية من 10 جزيئات مختلفة وهي جزيئتين ثنائي الأكسجين و 8 جزيئات ثنائي الأزوت ، و لحساب نسبتهما ننجز العملية التالية:
نسبة جزيئات ثنائي الأكسجين هي :
2 / 10 x 100% = 20%
نسبة جزيئات ثنائي الأزوت هي :
8 / 10 x 100% = 80%
ما هو مفهوم الذرة؟
الذرة (atome) هي عنصر كروي الشكل دقيق جدا لا يمكن رأيته بالعين المجردة ، يقاس قطرها بالنانومتر (nm) ، و تدخل في تركيب الجزيئة المكونة للمادة الصلبة أو السائلة أو الغازية.، و يمثل شكلها بالنموذج الذري.

|
| مفهوم الذرة |
ما هو النموذج الذري؟
تمثل الذرات بأشكال كروية مختلفة الحجم و اللون تسمى بالنموذج الذري (modèle atomique)، بحيث لكل نوع من الذرات نموذج خاص به حجمه يتناسب مع الحجم الحقيقي للذرة و له لون اصطلاحي يشير له، لاحظ الصورة التالية.

|
| النموذج الذري |
رموز الذرات
يرمز لكل ذرة برمز كيميائي خاص بها ، و هو الحرف الأول من اسمها اللاتيني ، و في بعض الأحيان يضاف له حرف اخر يكتب بشكل صغيرا كذرة الكلور Cl و ذرة الكربون C، و ذلك تجنبا للخلط بين الرموز الذرية التي لها نفس الحرف الأول ، لاحظ الجدول التالي
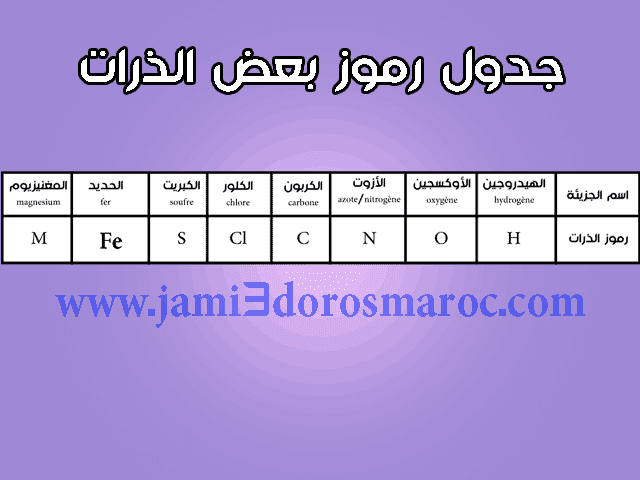
جدول رموز بعض الذرات
|
| جدول رموز بعض الذرات |
- ذرة الهيدروجين (hydrogène) : H
- ذرة الأكسجين (oxygène) : O
- ذرة الأزوت (azote/nitrogène) : N
- ذرة الكلور (chlore) : Cl
- ذرة الكربون (carbone) : C
- ذرة الكبريت (soufre) : S
- ذرة الحديد (fer) : Fe
- ذرة المغنيزيوم (magnésium) : M
الصيغة الكيميائية للجزيئة
يعبر عن الجزيئة بصيغة كيميائية (Formule chimique) نحصل عليها بكتابة رموز كافة الذرات المكونة لها جنبا الى جنب ، ثم نكتب عدد كل نوع من الذرات أسفل يمين رمزها ، كما في الأمثلة التالية.

|
| الصيغة الكيميائية للجزيئة |
الجزيئات التي تتكون من ذرتين لهما نفس النوع أو مختلفين تسمى جزيئات ثنائية الذرة molécules diatomiques ، أما الجزيئات المكونة من أكثر من ذرتين فتسمى جزيئات متعددة الذرات molécules polyatomiques ، بينما الجزيئات المكونة من ذرة واحدة تسمى جزيئات أحادية الذرة molécules monoatomiques.
تنبيه! في الصيغة الجزيئية ، لا يجوز كتابة العدد 1 أسفل يمين رمز الذرة التي عددها واحد ، و لا يجب كتاب عدد الذرة يسار رمزها بل يجب كتابته أسفل يمينها كما في الأمثلة أعلاه، على سبيل المثال الرمز H₂ خاص بثنائي الهيدروجين و هي جزئية تتكون من ذرتين هيدروجين متحدتين ، بينما الرمز 2H يشير الى تواجد ذرتين هيدروجين منفصلتين.
كيفية ترتيب الرموز في الصيغة الكيميائية؟
عند كتابتك لصيغة كيميائية لجزئية معينة ، فيجب أن يكون ترتيبك لرموز الصيغة صحيح ، و ذلك بالتعرف على العناصر الأقل فلزية وهي العناصر التي تنتهي اسمائها بحرفي (يد) مثل أوكسيد (Oxyde) المنتمي للأوكسجين أو كلوريد (Chlorure)المنتمي للكلور أو هيدريد (Hydrure) المنتمي للهيدروجين ، العنصر الأكثر فلزية يكون موضعه في الصيغة قبل العنصر الأقل ، بمعنى أبسط في الغالب عندما تجد جزيئة أحد مكوناتها ينتهي اسمه ب(يد) يجب أن يكون موضع رمزه بعد رمز العنصر الاخر ، مثال جزيئة أوكسيد ثنائي الهيدروجين (monoxyde de dihydrogène) تتكون من ذرة O و ذرتين H و بما أن ذرة الأكسجين O اسمها ينتهي بحرفي (يد) فسيكون موضع رمزها بعد H بهذا الشكل H₂O.
الجسم البسيط و الجسم المركب
الجسم البسيط (Cops simple) هو جسم خالص (corps pur)، ذو جزئيات تتكون من ذرات لها نفس النوع.
أمثلة عن الأجسام البسيطة
- ثنائي الهيدروجين dihydrogène صيغته الكيميائية H₂.
- ثنائي الأكسجين dioxygène صيغته الكيميائية O₂.
- ثنائي الأزوت diazote صيغته الكيميائية N₂.
أمثلة عن الأجسام المركبة
- أوكسيد ثنائي الهيدروجين وهو الماء monoxyde de dihydrogène صيغته الكيميائية H₂O.
- ثنائي أوكسيد الكربون dioxyde de carbone صيغته الكيميائية CO₂.
- أحادي أكسيد الكربون monoxyde de carbone صيغته الكيميائية CO.
فيديو الجزيئات والذرات للسنة الثانية اعدادي
- ملحقات الدرس